Faktor yang Mempengaruhi Laju Reaksi – Laju reaksi merupakan salah satu konsep dasar dari Kimia yang membahas mengenai perubahan konsentrasi suatu reaktan atau produk dalam satuan waktu. Laju reaksi sendiri yang dinyatakan dalam persamaan laju reaksi yang dipengaruhi oleh berbagai faktor .
Menurut Raymond Chang dalam bukunya yang berjudul “Chemistry 10th Edition”, laju reaksi adalah perubahan konsentrasi suatu reaktan atau produk dalam satuan waktu. Laju reaksi memiliki satuan M/s (Molaritas per detik), menggambarkan perubahan konsentrasi (molaritas) suatu zat dalam waktu tertentu.
Saat terjadi reaksi kimia, hal yang terjadi adalah pengurangan konsentrasi zat yang bereaksi (reaktan) karena telah menjadi produk dan menyebabkan konsentrasi produk bertambah seiring berjalannya waktu. B
Faktor yang Mempengaruhi Laju Reaksi Kimia
Berikut ini adalah ilustrasi perubahan konsentrasi reaktan dan produk dalam satuan waktu.
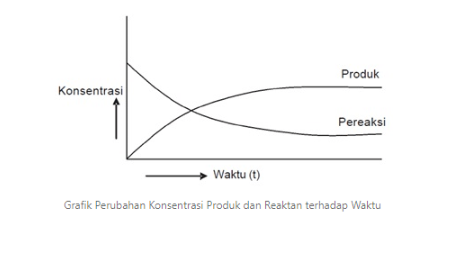
Dari gambar tersebut dapat diketahui bahwa pada saat awal sebelum terjadi reaksi, hanya terdapat reaktan dan belum ada produk. Saat reaksi mulai berjalan, konsentrasi reaktan akan menurun, dan konsentrasi produk akan bertambah seiring berjalannya waktu hingga reaksi selesai. Reaksinya adalah sebagai berikut.

Dimana ∆[A] adalah perubahan konsentrasi reaktan A, memiliki nilai negatif karena nilainya berkurang, dan ∆[B] adalah perubahan konsentrasi produk B yang bertambah, dalam perubahan waktu (∆t) tertentu.
Ketika kita sudah mengetahui bahwa laju reaksi merupakan perubahan konsentrasi suatu reaktan dan produk dalam satuan waktu, kemudian timbullah pertanyaan baru, “mengapa suatu reaksi kimia dapat terjadi hingga menyebabkan perubahan dari reaktan menjadi produk?”. Nah, untuk menjawab ini, kita akan berkenalan dengan Teori Tumbukan.
Teori Tumbukan
Suatu reaksi kimia dapat terjadi apabila molekul-molekul reaktan bertumbukan satu sama lain dengan orientasi yang tepat dan memiliki energi yang cukup. Pada teori tumbukan, syarat yang harus dipenuhi agar suatu reaksi kimia dapat terjadi adalah:
- Molekul-molekul harus saling bertumbukan (berinteraksi)
- Molekul-molekul yang bertumbukan memiliki energi yang cukup, melebihi energi aktivasi (Ea) dari reaksi yang akan dijalani
- Molekul-molekul yang bertumbukan harus pada orientasi yang tepat
Faktor yang Mempengaruhi Laju Reaksi Konsentrasi
Setelah diketahui bahwa reaksi kimia dapat terjadi karena adanya tumbukan-tumbukan antar molekul reaktannya, besarnya laju dari suatu reaksi kimia juga dipengaruhi oleh beberapa faktor. Faktor-faktor yang mempengaruhi laju reaksi adalah konsentrasi, temperatur, luas permukaan, dan katalis.
- Konsentrasi
Konsentrasi adalah salah satu hal yang mempengaruhi laju reaksi. Semakin besar konsentrasi reaktan, maka laju reaksi juga akan semakin besar.
Hal ini disebabkan karena konsentrasi yang besar menandakan bahwa molekul-molekul dalam suatu zat juga menjadi lebih banyak, banyaknya molekul-molekul tersebut juga memperbesar peluang adanya tumbukan yang menyebabkan reaksi dapat terjadi.
- Temperatur
Temperatur juga merupakan hal yang mempengaruhi laju reaksi. Temperatur yang lebih tinggi akan menyebabkan molekul-molekul lebih cepat dan bergerak sehingga menyebabkan molekul-molekul akan lebih sering bertumbukan dan memiliki energi yang lebih tinggi agar reaksi kimia dapat terjadi.
Temperatur yang lebih tinggi akan membuat laju reaksi menjadi lebih besar.Temperatur Terhadap Laju Reaksi.
- Luas Permukaan
Luas permukaan juga merupakan salah satu faktor yang mempengaruhi laju reaksi. Contoh mudah dari pengaruh luas permukaan terhadap laju reaksi adalah gula pasir dan gula batu.
Pada kondisi (temperatur dan berat) yang sama, gula pasir akan lebih cepat melarut dalam air dibandingkan dengan gula batu, hal ini disebabkan gula pasir memiliki luas permukaan yang lebih besar dibandingkan gula batu.
Maka dari itu, luas permukaan yang lebih besar akan menghasilkan laju reaksi yang lebih besar (reaksi lebih cepat terjadi).
- Katalis
Katalis juga dapat mempengaruhi laju reaksi, yaitu membuat laju reaksi semakin besar atau mempercepat laju reaksi.
Katalis bekerja dengan cara menurunkan energi aktivasi dari suatu reaksi sehingga energi yang diperlukan oleh molekul-molekul reaktan untuk bereaksi menjadi lebih rendah, dan reaksi lebih cepat atau mudah terjadi.
Katalis dapat menurunkan energi aktivasi dengan cara bereaksi dengan reaktan membentuk suatu kompleks teraktivasi, lalu akan terurai kembali membentuk produk dan mengembalikan katalis. Berikut ini adalah kurva energi reaksi dengan katalis maupun tanpa katalis.
Demikianlah penjelasan tentang Faktor yang Mempengaruhi Laju Reaksi. Semoga artikel ini bisa menambah pemahaman kita semua tentang laju reaksi.